- elemeket
- absztrakt
- hipotézis:
- mód:
- az eredmények:
- következtetés:
- bevezetés
- Tantárgyak és módszerek
- elemeket
- Klinikai paraméterek
- Vérminták
- Statisztikai elemzések
- az eredmény
- Az (OH) D hiány alacsonyabb inzulinérzékenységgel jár
- (OH) D-hiány a keringő gyulladásos mediátorok megemelkedett szintjéhez kapcsolódik
- A gyulladásos mediátorok összesítése 25 (OH) D-hiányos elhízott gyermeket különböztet meg
- vita
- További információ
- PDF fájlok
- További információ
elemeket
- Kalcium és D-vitamin
- gyulladás
- Elhízottság
- gyermekgyógyászat
absztrakt
hipotézis:
A gyermekkori elhízás alacsonyabb fokú szisztémás gyulladással jár, amely hozzájárul az inzulinrezisztencia és a szív- és érrendszeri szövődmények kialakulásához a későbbi életben. Mivel a D-vitaminnak mély immunmoduláló funkciói vannak, és a D-vitamin-hiány nagyon elterjedt a gyermekkori elhízásban, feltételeztük, hogy a gyermekkori elhízás D-vitamin-hiánya időben egybeesik a fokozott szisztémás gyulladással és az inzulinérzékenység csökkenésével.
mód:
Egy 64 elhízott és 32 egészséges, 6–16 éves egészséges gyermek keresztmetszeti vizsgálatában 32 keringő gyulladásos mediátor átfogó profilozását végezték el, a 25-hidroxi-D-vitamin (25 (OH) D) szintjének értékelésével és az inzulin mérésével együtt. érzékenység.,
az eredmények:
A súlyos D-vitamin-hiányt (a továbbiakban: D-vitamin-hiány) 25 (OH) D 37, 5 nmol 1 –1 szintként határozták meg, és nagyon elterjedt az elhízott (56%), szemben az egészséges kontrollokkal (16%)., A teljes vizsgálat 25 D (OH) D-hiányos gyermeket hasonlított össze más gyerekekkel, ebből 25 gyermek 25 (OH) D-hiányban (37, 5–50 nmol l –1) és 25 gyermek (OH) D-hiányban szenvedett ( 50 nmol l –1)). Először is, 25 (OH) D-hiányos elhízott gyermek inzulinérzékenysége alacsonyabb volt, mint más elhízott gyermekeknél, az inzulinérzékenység-kontroll alacsonyabb kvantitatív indexével mérve. Másodszor, a 25 (OH) D hiány és az inzulinrezisztencia közötti összefüggést gyermekkori elhízásban többszörös regressziós elemzés is megerősítette. Harmadszor, 25 (OH) D-hiányos elhízott gyermeknél magasabb volt a gyulladásos mediátorok katepszin S, kemerin és oldható vaszkuláris adhéziós molekula (sVCAM) szintje, mint más elhízott gyermekeknél. Végül a hierarchikus klaszteranalízis a 25 (OH) D hiány hiányának túlreprezentációját tárta fel olyan elhízott gyermekeknél, akik magas szintű katepszin S, sVCAM és kemerin gyulladásos mediátorok csoportjait fejezték ki.
következtetés:
A gyermekkori elhízás 25 (OH) D hiánya fokozott szisztémás gyulladással és csökkent inzulinérzékenységgel járt. A katepszin S és az sVCAM magas szintje tükrözheti a gyulladásgátló, a diabéteszes és az aterogén útvonalak aktiválódását, amelyet a D-vitamin pótlása gátolhat.
A D-vitamin kulcsfontosságú tápanyag, amely a csontanyagcserén kívül különféle fiziológiai folyamatokban vesz részt. A D-vitamin sokoldalúságát a D-vitamin receptor kiterjedt expressziója és a 25-hidroxi-D-vitamin (25 (OH) D), a D-vitamin elsődleges keringő formájának biológiai aktívvá történő átalakulásának molekuláris mechanizmusa szemlélteti. 25-dihidroxi-D-vitamin. 1,2 V Kulcsfontosságú tápanyagként betöltött szerepének megfelelően a 25 (OH) D (-1) hiányos szintje különböző betegségekhez kapcsolódik, beleértve a gyulladásos bélbetegségeket, a fertőző betegségeket és a szív- és érrendszeri rendellenességeket., 1, 2, 3 A közelmúltban összefüggés van a 25. hiány (OH) D és az elhízott gyermekek csökkent inzulinérzékenysége között. 4 A felnőtt lakosság körében végzett kiterjedt és prospektív kohorszvizsgálat rámutatott a 25 (OH) D hiány és a 2-es típusú cukorbetegség kialakulása közötti kapcsolatra. 5.
Mivel a magasabb testtömeg-index (BMI) a 25 (OH) D alacsonyabb szintjéhez vezet, feltehetően a zsírszövetben a D-vitamin megkötésével, a 625 (OH) D-hiány gyermekkori elhízásban endémiás. 4 A súlyos 25 (OH) D hiány (a továbbiakban: 25 (OH) D hiány) következményeinek vizsgálatához a 25 (OH) D hiányt a 25 (OH) D 37,5 nmol l - 1 szintjeként határoztuk meg. korábbi tanulmányoknak megfelelően. 7, 8, 9, 10 Meglepő módon az elhízott gyermekek 51% -ának az Egyesült Államokban 25 (OH) D hiánya van, szemben az Egyesült Államok összes gyermekének 9% -ával. 8.
(OH) D-hiány számos módon befolyásolhatja a glükóz homeosztázisát. Először is, mivel a D-vitamin kulcsszerepet játszik a kalcium-anyagcserében, és az inzulinszekréció kalciumfüggő folyamat, a 25 (OH) D hiányáról azt gondolták, hogy kalciumfüggő módon gátolja a β-sejtek inzulinszekrécióját. 11 Másodszor, 25 (OH) D hiány a perifériás inzulin hatásának csökkenésével, vagy az inzulin receptor expressziójának csökkenésével, vagy a downstream inzulin jelátvitel csökkenésével járt. 11 Harmadszor, a D-vitamin jól ismert immunmoduláló funkcióiról. Figyelembe véve a szisztémás gyulladásnak az elhízás 13 inzulinrezisztenciájára gyakorolt káros hatásait, azt javasolták, hogy a 25 (OH) D-hiány fokozott szisztémás gyulladással rontja az elhízás inzulinrezisztenciáját. 11, 14
Itt a második hipotézisre koncentrálunk. Egy keresztmetszeti vizsgálatban 64 egészséges kontroll gyermek, elhízás, életkor és nem, az életkornak és a nemnek megfelelően elemeztük a keringésben lévő 25 (OH) D és 32 szisztémás gyulladásos mediátor szintjét, valamint az inzulinérzékenység arányát. Tudomásunk szerint ez az első olyan vizsgálat, amely a gyulladásos mediátorok átfogó profilozását végezte el a 25 (OH) D státusszal kapcsolatban, és megmutatta, hogy a gyermekkori elhízás 25 (OH) D hiánya csökkenő inzulinérzékenységgel és fokozott szisztémás gyulladással jár.
Tantárgyak és módszerek
elemeket
A gyermekkori elhízás definíciója: BMI> 2,5 sd, átlag életkor és nem szerinti BMI (BMI-sd), összhangban a gyermekkori elhízás nemzetközi definíciójával, mint 30 kg m - 2-es BMI, amelyet az életkor tükröz. 18 év. 13, 15, 16 Egy keresztmetszeti vizsgálatban 64 elhízott gyermeket és 32 egészséges kontrollt életkor és nem szerint, BMI-sd –1-vel vontak be a Meander Medical Center gyermek ambulanciájába (
15 ng ml –1), 25 (OH) D hiányt 25 (OH) D szintként határoztunk meg, 37,5 és 50 nmol közötti l –1 (15–20 ng ml –1) és 25 (OH) D szintet 50 A nmol l –1 elegendőnek minősült a korábbi vizsgálatok és a nemzetközi irányelvek szerint. 3, 7, 8, 9, 10, 17 Egy 25 (OH) D hiányban szenvedő beteg és egy kellően elhízott beteg számolt be orális inzulinérzékenyítők (metformin) szedéséről. Egyik gyermek sem számolt be a 25. kiegészítés (OH) D használatáról. Minden gyermektől és szüleiktől írásos tájékoztatáson alapuló beleegyezést kaptak. A tanulmányt az Etikai Felülvizsgálattal foglalkozó Intézményi Orvosi Bizottság hagyta jóvá (METC 09/217K).
Klinikai paraméterek
A bioelektronikus impedancia (teljes testzsírszázalék) mérésére egy láb bioimpedancia-analizátort használtunk a gyártó utasításai szerint (Analyzer Model BIA 101; Akern Srl, Firenze, Olaszország). A bőr tónusa világosra, közepesre és sötétre oszlott. 18 A nemek és a nemek közötti korosztályi nemet Cole LMS módszerével és a Holland Nemzeti Növekedési Tanulmány adatai alapján számoltuk ki. 16, 19
Vérminták
A vérmintákat egy éjszakán át tartó gyors nátrium-heparin csövekbe vettük. A 25 (OH) D-szinteket az Elecsys D-vitamin teljes assay segítségével mértük, amely mind a 25 (OH) D2, mind a 25 (OH) D3-at (Roche Diagnostics, Mannheim, Németország) méri. Az alulkarboxilezett és karboxilezett oszteokalcin szinteket ELISA kitek segítségével határoztuk meg (Takara MK111 és MK118, Takara Bio USA, Madison, WI, USA). Az összes oszteokalcin szint a karboxilezett és az elégtelenül karboxilezett oszteokalcin összegét jelenti. A rutin laboratóriumi vizsgálatok magukban foglalták az éhomi glükózt, az éhomi inzulint, a triglicerideket, a magas és alacsony sűrűségű lipoprotein koleszterint (HDL és LDL), valamint a nagyon érzékeny C-reaktív fehérjék (hsCRP) szintjét. A kvantitatív inzulinérzékenység-kontroll indexet (QUICKI) és az inzulinrezisztencia homeosztázis modell (HOMA-IR) kiértékelését a korábban leírtak szerint számítottuk. A keringésben lévő gyulladásos mediátorokat a közelmúltban kifejlesztett és validált multiplex immunvizsgálattal mértük a plazmában. 22.
Statisztikai elemzések
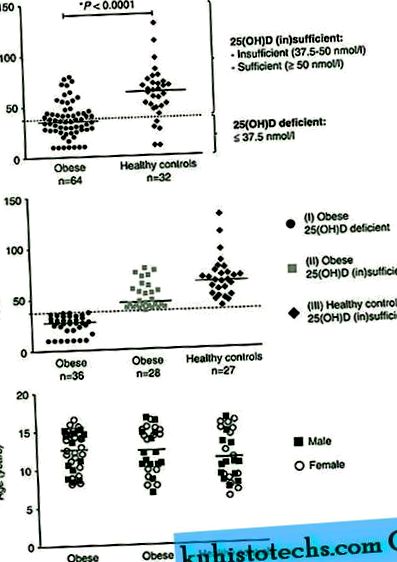
A cikkben 25 (OH) D-hiányos elhízott gyermeket (n = 36) hasonlítottak össze (elegendő) elhízott gyermekkel (n = 28), hogy tanulmányozzák a nagyon alacsony 25 (OH) D-szint hatását elhízottaknál gyermekek. Ezen túlmenően az elhízás hatásainak tanulmányozásához az elhízott gyermekek (nem) számát hasonlították össze az elégtelen egészséges kontrollokkal (n = 27). Felhívjuk figyelmét, hogy öt, az egészséges kontroll hiányában szenvedő gyermeket kizártak a további elemzésekből, mivel ezt a csoportot túl kicinek tartották ahhoz, hogy összehasonlítsák az elégtelenül elhízott gyermekekkel (1. ábra).
25 (OH) D-hiány elhízott gyermekeknél. a ) Az elhízott gyermekek 25 (OH) D szintje (n = 64) és az egészséges kontrollok (n = 32), amelyek lényegesen alacsonyabb 25 (OH) D szintet mutatnak az elhízott gyermekeknél. A súlyos 25 (OH) D hiányt, amelyet 25 (OH) D hiánynak neveznek, 25 (OH) D szintként definiálják
37, 5 nmol 1 –1 a korábbi tanulmányoknak és a nemzetközi irányelveknek megfelelően. Az egész cikk 25 D (25) hiányos gyermeket hasonlít össze D (25 (OH) D hiányban 37, 5–50 nmol 1 –1) és 25 gyermeket 25 (OH) D (25 (OH) OH) D hiányban = 50 nmol 1-1). b ) Az elhízott hiányos gyermekek 25 (OH) D szintje (I. csoport, n = 36), (in) elegendő számú elhízott gyermek (II. Csoport, n = 28) és (in) elegendő számú egészséges kontroll (III., N csoport) = 27))). A cikkben a csoportokat a következőképpen hasonlítottuk össze: (1) elégtelen elhízott gyermekek versus (v) elegendő elhízott gyermekek ahhoz, hogy tanulmányozzák a nagyon alacsony 25 (OH) D-szint hatását elhízott gyermekeknél és (2) (elégtelen) elhízott gyermekeknél versus (nem megfelelő egészséges kontrollok az elhízás hatásának tanulmányozásához. Felhívjuk figyelmét, hogy öt, az egészséges kontroll hiányában szenvedő gyermeket kizártak a további elemzésekből, mivel ezt a csoportot túl kicinek tartották ahhoz, hogy összehasonlítsák az elégtelen elhízott gyermekekkel. c ) A három csoport életkor és nem szerinti megoszlása. Panelhez a - c a mediánvonalakat képviselik.
Teljes méretű kép
Mivel a legtöbb klinikai paraméter és gyulladásos mediátor nemparametrikus eloszlást mutatott, a csoportok közötti különbségek értékeléséhez Mann-Whitney U-tesztet vagy Fisher pontos tesztet használtak. Benjamini és Hochberg téves felfedezésének kijavítását használták a P-értékek korrigálására többszörös tesztelés során. Többszörös lineáris regressziós analízist végeztünk a QUICKI státusz és a 25 (OH) D kapcsolatának vizsgálatára, korrigálva a BMI-sd, az életkor, a nem, a bőr tónusa és az elégtelenül karboxilezett osteocalcin értékekkel. Ehhez hasonlóan értékelték a gyulladás mediátorainak és a 25 (OH) D státusz közötti kapcsolatot, korrigálva a BMI-sd-t, az életkorot és a nemet.
A statisztikai elemzéseket az SPSS 15.0 for Windows (SPSS, Chicago, IL, USA) és az R, a statisztikai számítások és grafikák szabad szoftveres környezetével végeztük. A gyulladásos mediátorprofilok nem ellenőrzött hierarchikus klaszteranalízisét végeztük el, a közelmúltban leírtak szerint, 13 a Pvclust csomag felhasználásával. 24.
az eredmény
Az (OH) D hiány alacsonyabb inzulinérzékenységgel jár
A 25 (OH) D hiány 56% -os prevalenciát mutatott az elhízott gyermekeknél, szemben az egészséges gyermekek 16% -ával (1. táblázat, 1a. Ábra). A 25 (OH) D elhízott gyermekek állapota relevánsnak tűnt, mivel az elhízott gyermekek hiányosságai (azaz 25 (OH) D hiány, n = 36) alacsonyabb inzulinérzékenységet mutattak, mint elegendő számú elhízott gyermek (azaz 25 (OH) D )) D (in) elégséges, n = 28), alacsonyabb QUICKI és magasabb HOMA-IR értékekkel mérve (1. táblázat, 1b ábra), amelyek az inzulinérzékenység helyettesítő markerei. Az inzulinérzékenység különbségei nem magyarázhatók olyan klinikai paraméterekkel, mint az életkor, a nem, a BMI-sd, az sd sáv kerülete (zsigeri adipozitási ráta 25), a zsírszázalék, a lipidprofil és az inklúziós időszak, amelyek mind összehasonlíthatók voltak az elégtelen és ( in) elegendő számú elhízott gyermek (1. táblázat, 1c. ábra).
Asztal teljes méretben
Asztal teljes méretben
Az elhízás 25 (OH) D-hiánytól független hatásának tanulmányozásához a keringő gyulladásos mediátorok közötti különbségeket is értékelték az elhízott és egészséges gyermekek (elégtelen) száma között. Magasabb interleukin-18 (IL-18), májnövekedési faktor (HGF), leptin, epidermális növekedési faktor (EGF) és tumor nekrózis faktor 2 receptor (TNF-R2) magasabb szintje és alacsonyabb szintű tumor nekrózis faktor (TNF-R2) elegendő számú elhízott gyermeknél figyeltek meg 1. plazminogén aktivátor inhibitor (PAI-1) (2. táblázat). Többszörös tesztelés céljából végzett korrekció után a leptin, az EGF, a TNF-R2 és a PAI-1 különbségei továbbra is szignifikánsak maradtak, míg az IL-18 és a HGF trendet mutatott (P = 0,07, illetve 0,05). Összességében a 25 (OH) D hiány hiányának a keringő gyulladásos mediátorokra gyakorolt hatása a gyermekkori elhízásban különbözött magától az elhízás hatásától. Bár az elhízás a leptin, az EGF, a TNF-R2, a PAI-1, az IL-18 és a HGF megváltozott szintjével társult, egy nemrégiben készült tanulmánynak megfelelően, a gyermekkori elhízás 1325 (OH) D hiánya egybeesett a katepszin S magasabb szintjével kemerin, RBP-4 és sVCAM.
Az IL-6, IL-10 és TNF-a citokinek esetében; adipokinek adiponektin, adipszin, zsírsavat kötő 4-es fehérje (FABP-4), makrofág-migrációt gátló faktor (MIF), monocita kemotaktikus protein-1, (CCL2), omentin, gyanta, szöveti metalloproteináz 1-gátló (TIMP-1) és trombopoietin; és egyéb gyulladásos mediátorok kemokin (CXC motívum) ligand-8 (CXCL8), extracelluláris újonnan azonosított RAGE-kötő fehérje (EN-RAGE), IFN-gamma által indukált protein 10, (CXCL10), makrofág kolónia stimuláló faktor (M-CSF) ), makrofág gyulladásos fehérje 1a, (CCL3), makrofág gyulladásos fehérje 1p, (CCL4), oldható CD14, oldható intercelluláris adhéziós molekula (sICAM), TNF 1 receptor (TNF-R1) és vaszkuláris endoteliális növekedési faktor (VEGF), nincs különbség 25 (OH) D-hiányos és (elégtelen) elhízott beteg között, vagy elégtelen elhízott és egészséges gyermekek között találtak (2. kiegészítő táblázat).
A többszörös lineáris regresszióanalízis minden gyermeknél alátámasztotta a katepszin S, kemerin és sVCAM 25 (OH) D függőségét: a katepszin S és az sVCAM a 25 (OH) D státustól függ, bár a BMI-sd, az életkor és a nem szempontjából igazították, míg a kemerin szint a 25 (OH) D függőség felé mutató tendenciát mutatott (P = 0,08; 2. táblázat). Az RBP-4 szintek nem függtek a 25 (OH) D állapottól, miután beállítottuk a fent említett lehetséges zavarokat (P = 0,160). Összegzésképpen elmondható, hogy a gyermekkori elhízás 25 (OH) D hiánya összefüggésben van a keringő gyulladásos mediátorok, nevezetesen a katepszin S, a kemerin és az sVCAM megnövekedett szintjével.
A gyulladásos mediátorok összesítése 25 (OH) D-hiányos elhízott gyermeket különböztet meg
A 25 (OH) D hiány és gyulladás közötti összefüggés vizsgálatának alternatív megközelítéseként az elhízott gyermekek gyulladásos mediátor profilját hierarchikus klaszteranalízisnek vetették alá. Érdekes módon a katepszin S és az sVCAM, a 25 (OH) D hiányhoz legerősebben társuló gyulladásos mediátorok (lásd fent) 65% -os bootstrap valószínűséget mutattak, ami robusztus csoportosulást jelzett (2a. Ábra). 13 TIMP-1, leptin, kemerin, rezisztin, sICAM és PAI-1 mellett gyulladás-mediátor klasztert is tartalmaztak, amelyek elhízott gyermekek két klaszterét különböztették meg (2b. Ábra). Az I. klaszter vegyes csoportot képviselt, beleértve a hiányos és hiányos gyermekeket. A II. Klaszter túlnyomóan elhízott gyermekeket tartalmazott (P = 0,008). Összességében a gyulladásos mediátorok klaszteranalízise aláhúzta a kapcsolatot a 25 (OH) D hiány és a gyulladás között. Elhízott gyermekeknél, akiknél a gyulladásos mediátorok csoportjai expresszálódtak magas katepszin S, sVCAM és kemerin szinttel, a 25 (OH) D hiányt felülreprezentálták.
Teljes méretű kép
vita
Különösen ez a tanulmány nem zárja ki a 25 (OH) D hiány kalciumfüggő hatását az inzulinreceptor expressziójára vagy jelátvitelére, mivel ezeket a paramétereket nem vizsgálták. Továbbá, mivel a 25 (OH) D-hiányos egészséges kontrollok száma túl kicsi volt ahhoz, hogy a későbbi elemzésekbe belefoglalják (n = 5, 1a. Ábra), ez a tanulmány kifejezetten a 25 (OH) D-hiány elhízott gyermekekre gyakorolt hatására összpontosított. . További vizsgálatot igényel, hogy a 25 (OH) D hiányosság a nem elhízott gyermekeknél fokozott szisztémás gyulladással is jár-e. Továbbá, ebben a vizsgálatban nem figyeltek meg táplálékfelvételt, kültéri aktivitást és testmozgást, ami hatással lehet a 25 (OH) D 8 minden szintjére. Végül keresztmetszeti elrendezése miatt még nem sikerült ok-okozati összefüggést megállapítani a fokozott szisztémás gyulladás és az inzulinrezisztencia között. Ebből a célból leendő tanulmányokra van szükség. A koncepció tanulmány tanulmányaként azonban adataink új betekintést nyújtanak azokba a kórélettani mechanizmusokba, amelyek a 25 (OH) D hiányt összekapcsolhatják az inzulinrezisztenciával. Ezenkívül ez a tanulmány kiemeli a gyermekkori elhízás 25 (OH) D hiányának következményeit, amelyek a jelek szerint csak a kalcium anyagcserére és a csontok növekedésére gyakorolt hatásokat jelentik. 2, 7
- A hétvégi alváshiány gyermekkori elhízáshoz vezet - Egészség és megelőzés - Egészség
- Az alváshiány elhízáshoz vezet - 2021-es betegség
- A laktázhiány, mint a gyermekkori kólika egyik fő oka
- Az alváshiány elhízáshoz vezethet - Egészség és Megelőzés - Egészség
- B 12-vitamin hiány és felesleg Mi a veszélyesebb? Kiegészítjük a testet B 12-vitaminnal -