- absztrakt
- A fő
- ANYAGOK ÉS METÓDUSOK
- betegek
- Multiplexes ligációs szonda amplifikációja
- Fluoreszcencia in situ hibridizáció
- AZ EREDMÉNYEK
- A beteg
- B beteg
- C beteg
- D beteg
- VITA
absztrakt
Cél: A veleszületett rendellenességek az újszülöttek morbiditásának és halálozásának fő okai, és a genomi egyensúlyhiány etiológiájuk fontos része. Ennek a vizsgálatnak az volt a célja, hogy értékelje a prenatális multiplex ligációs szonda amplifikációs képernyőjének azon képességét, hogy ismeretlen etiológiájú ultrahang-rendellenességekkel rendelkező magzatokban rejtett kromoszóma-egyensúlyhiányokat detektáljon.
Módszerek: A multiplex ligációs próba amplifikációját három különálló próbakészlettel hajtottuk végre: kettőt szubtelomer régiókhoz és egyet mentális retardációs szindróma lokuszokhoz. A 2007 januárjától 2009 januárjáig terjedő időszakban hatvanegy magzatot teszteltek jelentős ultrahang anomáliákkal és normál kariotípussal, legalább 400 sáv felbontásával.
Eredmények: Négy kiegyensúlyozatlan elrendezést azonosítottunk: egy del 18pter/amp 5pter, egy del 9pter, egy 15q11q13 és egy 22q11 mikrodeleton atipikus megjelenítéssel. Genetikai tanácsadás után két terhességet megszakítottak.
Következtetés: A multiplex ligációs próba amplifikációs elemzése képes volt klinikailag szignifikáns változásokat azonosítani a prenatálisan azonosított sonográfiai rendellenességekkel rendelkező magzatok 6,5% -ában. Ez a prospektív tanulmány hangsúlyozza, hogy a magzati amplifikáció szűrése ultrahang-rendellenességekkel a prenatális időszakban a multiplex amplifikációs szonda szűrése, amely technikailag megvalósítható és releváns a diagnózis és a prognózis szempontjából.
A fő
A veleszületett rendellenességek az újszülöttek morbiditásának és halálozásának fő okai, és a lakosság körülbelül 3% -ánál diagnosztizálják őket. Néhány veleszületett rendellenességet ultrahanggal detektálnak a prenatális időszakban. A chorionus villus mintavételezéssel vagy az amniocentézissel nyert standard kariotípus az érintett magzatok 18–35% -ában tárja fel a kromoszóma-rendellenességeket. 1, 2 Fluoreszcens in situ hibridizáción (FISH), összehasonlító genomi hibridizáción (metafázis terjedés vagy CGH mező) és kvantitatív multiplex polimeráz láncreakció (PCR) módszereken, például multiplex amplifikáción alapuló nagy felbontású módszereket alkalmaznak ennek a kimutatási aránynak a növelésére. ligációs szonda. (MLPA) vagy rövid fragmensek kvantitatív multiplex PCR-je, de ezek használata a prenatális diagnózisban továbbra is korlátozott.
A telomer-specifikus feloma már hasznos eszköznek bizonyult a nagy rendellenességekkel járó magzatok delécióinak és duplikációinak kimutatására. 3, 4 Nemrégiben bevezetésre került a CGH magzati minták elemzése az alacsony kópiaszámú DNS-változások kimutatására. Az 5-8. Az MLPA gyors, költséghatékony módszer a mentális retardációval (mentális retardációs szindróma [MRS] -MLPA) összefüggő régiókban talált rejtélyes, kiegyensúlyozatlan szubtelomer átrendeződések és intersticiális egyensúlyhiányok szűrésére. Az MLPA valójában kevesebb mint 2 napot igényel, és az MLPA eredményei 3 napon belül (ha FISH-ellenőrzésre van szükség) 4 napon belül elérhetők lehetnek. Eddig csak egy tanulmány kombinálta az MRS-MLPA-t és a szubtelomer MLPA-t, ami 5,8% -ról 10,1% -ra javította az egyensúlyhiány észlelésének arányát a mentális retardációval küzdő gyermekeknél. 9.
Ez a tanulmány szubtelomer MLPA és MRS-MLPA alkalmazásával 61 normál kariotípusú és kromoszóma-rendellenességre utaló ultrahang-rendellenességet vizsgált magzatot vizsgált. Tudomásunk szerint ez az MRS-MLPA-val kombinált szubtelomer MLPA első jelentése, amelyet prenatális prospektív szűrési módszerként alkalmaznak az ultrahang-rendellenességekkel rendelkező magzatok diagnosztikai értékelésében.
ANYAGOK ÉS METÓDUSOK
betegek
Hatvanegy magzat, amelyek egy vagy több kromoszóma-rendellenességre utaló rendellenességgel és normális kariotípussal utalnak, bekerültek prospektív vizsgálatunkba 2007 januárjától 2009 januárjáig (1. táblázat). Minden magzathoz 400 sávos kariotípust végeztünk, magzatvízből vagy korionbolyhokból származó RHG és GTG átkötésével. Szív rendellenességek esetén a FISH 22q11.2-et végeztük. Amikor a kariotípus és a FISH eredmények normálisak voltak, azt javasoltuk, hogy a betegek folytassák a citogenetikai vizsgálatokat az MLPA alkalmazásával. Mind a 61 beteg beleegyezett abba, hogy részt vegyen a vizsgálatban, és megfelelő tájékozott beleegyezést kaptak. A tanulmány a Helsinki alapelveinek teljes betartásával készült.
Asztal teljes méretben
Multiplexes ligációs szonda amplifikációja
Százhúsz nanogramm DNS-t használtak fel az MLPA protokollban. A reakciókat egy TProfessional termocikluson hajtották végre (Biometra, Archamps, Franciaország). Három mikroliter PCR-terméket analizáltunk kapilláris elektroforézissel ABI Prism 3100 genetikai analizátoron (Applied Biosystems, Courtabeouf, Franciaország), és a kvantitatív adatokat kivontuk az ABI Prism GeneScan Analysis és Genetyper szoftverrel (Applied Biosystems). Az MLPA adatok elemzését Microsoft Excel segítségével végeztük el. Egy beteg kiegyensúlyozatlan t (10; 18) (qter; qter) transzlokációval és egy 15q12 delécióval rendelkező beteg pozitív kontrollként szerepelt minden MLPA P036/P070 és P245 vizsgálatban, egy negatív kontroll mellett. A kóros eredményeket úgy határoztuk meg, hogy a genetikai anyag nyeresége meghaladja az 1,3-ot, a veszteség esetében pedig az 0,7-et.
Fluoreszcencia in situ hibridizáció
Az MLPA által elért rendellenes eredményeket a FISH megerősítette metafázisos kromoszómákon szokásos eljárásokkal (Cytocell Technology vagy Vysis, Inc., Downers Grove, IL) a gyanús régiókban elhelyezkedő próbák és kontroll szondák alkalmazásával. A szülők perifériás vérének limfocitáit a FISH elemezte, amikor a magzat pozitív átrendeződését tesztelték.
AZ EREDMÉNYEK
Titkos egyensúlyhiányt találtunk az MLPA által vizsgált 61 magzat közül négyben (6,5%). Két szubtelomer átrendeződést és két pericentromer mikrodeletiót azonosítottunk. E négy eset klinikai és citogenetikai adatait az alábbiakban közöljük.
A beteg
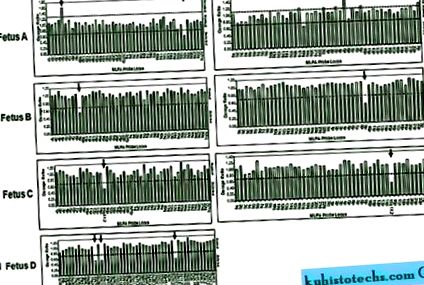
A szubtelomer MLPA és az MRS-MLPA géndózis-aránya. A, A SALSA P036 (balra) és P070 (jobbra) készlet dózisaránya az A magzat számára, amely 5p telomer amplifikációt és 18q telomer törlést mutat. B, A SALSA próba dózisaránya P036 (balra) és P070 (jobbra) a B magzatnál, amely 9p telomer deléciót mutat. C, A SALSA próba dózisaránya P036 (balra) és P070 (jobbra) a magzat C esetében, a 15q11.2 régió delécióját mutatva. D, a SALSA P245 próbakészletek dózisaránya a magzat számára D három, a 22q11.21 régiót megcélzó próba törlését mutatja.
Teljes méretű kép
B beteg
Ennek a magzatnak a 26 éves édesanyja terhes volt második gyermekével. Az első trimeszter ultrahangvizsgálata 1,4 mm-nél mérte a nyaki áttetszőség vastagságát, és az anyai szérum szűrése becslést adott a Down-szindróma kockázatának 1: 840-re. A család története jelentéktelen volt. 34 hetes terhesség után az ultrahangvizsgálat intrauterin növekedési retardációt és hypospadiasokat tárt fel, ami az amniocentesis ajánlásához vezetett. A 46. kariotípus, XY normális volt, és a 4p16.3 delécióra vonatkozó FISH-vizsgálatok (Wolf-Hirschhorn, OMIM194190) negatívak voltak. Az MLPA szubtelomer analízise 9 pter veszteséget mutatott ki (1B. Ábra). A törlést a FISH megerősítette (lásd B. ábra, További digitális tartalom 2, //links.lww.com/GIM/A105). Az MLPA és a FISH által meghatározott minimális méret 810 Kb volt (DMRT1-, DOCK8-, RP11-143M15-). A szülők metafázis terjedésének kariotípus- és FISH-elemzése nem mutatott aberrációt. Tanácsadás után és a francia jogszabályoknak megfelelően a szülők úgy döntöttek, hogy a mentális retardáció magas kockázata miatt 38 hétre megszakítják a terhességet. A posztmortem klinikai értékelés megerősítette a hypospadiákat és felfedte az arc diszmorfizmusát fokozott hasítási pásztorokkal, mikroretrognathiával, rövid nyakkal és széles mellbimbókkal.
C beteg
D beteg
A páciens 30 éves primagravida volt. Az első trimeszterben a nyelőcső áttetszőségének vastagságát 1,6 mm-nél mértük, és az anyai szérumszűrés becslést adott az alsó szindróma 1: 2899 kockázatára. 25 hetes terhesség után az ultrahang egyoldalú diszpláziás multiciklusos veséket és kétoldali lábszárakat mutatott, amncenthez . A családtörténet jelentéktelen volt, és a szülők vese ultrahangvizsgálata normális volt. A magzati ketotípus, 46, XY, normális volt. 32 hetes terhesség után jelentős polihidramniókat detektáltak, és az MLPA-t krioprezervált sejteken végezték. Az MRS-MLPA 22q11, 2 (1D. Ábra) minimális 1,68 Mb méretű (CLDN5 -, GP1BB -, SNAP29 -) mikrodeletiót észlelt, amelyet a FISH is megerősített (lásd D ábra, 2. kiegészítő digitális tartalom, // linkek.lww. com/GIM/A105). A szülők nem voltak hajlandók elvégezni saját kariotípus-vizsgálatukat, és genetikai tanácsadás után úgy döntöttek, hogy folytatják a terhességet. A posztnatális értékelés a magzati rendellenességek során megerősítette a magzati rendellenességeket és további rendellenességeket. Ezek közé tartozik a perimembranos interventricularis kommunikáció, a gége stridorja és a súlyos gastrooesophagealis reflux. A súlya 3540 g, a hossza 50,5 cm, a tarkó elülső kerülete 36 cm.
VITA
Ennek a tanulmánynak az volt a célja, hogy értékelje az MLPA prenatális időszakban történő megvalósításának technikai megvalósíthatóságát és hasznosságát. Tudomásunk szerint ez az első tanulmány, amely az MRS-MLPA-t subtelomer MLPA-val kombinálva értékelte a magzatok prenatális diagnosztikai szűrésében, ismeretlen etiológiájú kóros ultrahanggal.
Négy szubmikroszkópos átrendeződést észleltünk három különböző MLPA-szonda segítségével 61 magzatban, amelyeket laboratóriumunkba küldtek abnormális ultrahang céljából. Ezt az egyensúlyhiányt a FISH megerősítette a metafázis terjedésekben.
Két intersticiális törlést is találtunk (3, 3%). A szubtelomer MLPA és az MRS-MLPA 15q11q13 mikrodeletiót mutatott ki, amely polihidramniózissal és hipotenzióval társult. Bigi és mtsai. 18 közzétette az első jelentést, amely leírta a PWS lehetséges magzati fenotípusát, amelyet 30 hetes terhesség után lehetett azonosítani. Azt állították, hogy a karok és lábak sajátos helyzete, amely a csökkent magzati mozgásokhoz és a polihidrammóniumhoz kapcsolódik, PWS-t jelez. 18 A C magzat azonban nem mutatta a végtagok ilyen jellegű eltérését. Dudley és Muscatelli 19 a PWS születési jellemzőinek genotípustól függő variációját írták le, azaz egy deléciót vagy az anyai uniparentális diszomiát, ami megnehezítette a magzati fenotípus meghatározását. Az MRS-MLPA egy 22q11,2 mikrodeletiót is észlelt atipikus megjelenéssel. A vesediszplázia gyakran társul a 22q11.2 mikrodeletióval, és ebben a szindrómában többféle polihidramniót és kullancsot jelentettek. 20, 21 Azonban tudomásunk szerint a D magzatban azonosított egyoldalú diszpláziás multiciklusos vesék, bilaterális klublábak és polihidramnionok prenatális társulásáról soha nem számoltak be a 22q11, 2 mikrodeletiós szindrómában. Ez a két eset együttesen arra utal, hogy az MRS-MLPA a mikrodeletióció hasznos felismerése atipikus vagy hiányos prenatális prezentációval.