elemeket
- Csontvelő-transzplantáció
- Sejtjelzés
- kemoterápia
- myeloma
Annak ellenére, hogy a mielóma multiplexben a közelmúltban jelentős terápiás fejlődés történt, a refrakter betegségek regressziója/progressziója, különösen az auto-SCT után, továbbra is kielégítetlen kihívás a területen. Genetikailag a REL gyakori mutációjáról számoltak be mielomában. 1 Ezenkívül az NRAS mutációban szenvedő betegeknél csökkent a bortezomib iránti érzékenység. 2 Ezért célzott anti-RAS aktivációs terápia. A sorafenib egy RAS-aktivációt célzó multi-kináz inhibitor. Másrészt a bortezomibról kiderült, hogy a refrakter mielómában helyreállítja az alkilátorokkal szembeni kemoszenzitivitást. 4 Ez a cikk olyan bortezomib és lenalidomid-refrakter myelomában szenvedő betegeket mutat be, akiknek ERK1/2 aktivációja van a V600E BRAF mutáció következtében, amelynek eredményeként a sorafenib tartós válaszreakciót eredményezett, de az ezt követő bortezomib/bendamustin/dexametazon (VBD) kombináció PR.
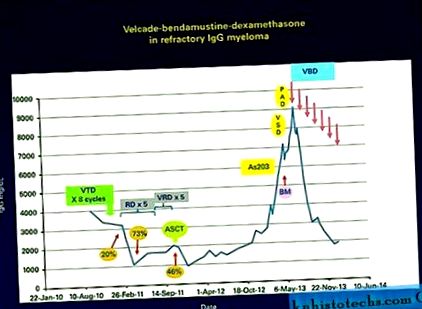
Kezelés és szérum IgG válasz a betegség folyamán. A páciens csak 20% paraprotein-választ ért el nyolc ciklus VTD és átmeneti, de tartós PR után az RD-n, amely végül rezisztens volt a VRD-vel szemben. Nagyon jó PR-értéket értek el az auto-SCT-vel, de a betegség 9 hónappal később előrehaladt, amelyben az As203/dex válasz nélkül indult. BM aspirációt hajtottak végre, amely konstitutív ERK aktiválódást mutatott ki, és ezért indokolatlanul kisebb válasz esetén indították el a VSD-n. A betegség a PAD megmentése ellenére is folytatódott, de elérte a PR-t a VBD-hez.
Teljes méretű kép
A páciens kariotípusa, RAS/RAF mutációja, RASSF1A metilációja és ERK1/2 aktiválása. (1q21). Az NRAS, a KRAS és a BRAF szekvenálása V600E BRAF mutációt mutatott. A metiláció-specifikus PCR azt jelzi, hogy a RASSF1A promoter (UU) nem metilálódik. A CD138-válogatott BM plazma sejtek Western blot elemzése kimutatta az ERK1/2. ++, foszfo-ERK1/2 pozitív aktiválódását; UU, nem metilezés; WT, vad típusú. A HeLa és a KMS-12-BM sejtek pozitív és negatív kontrollként szolgáltak az ERK aktiválásához.
Teljes méretű kép
Kimutatták, hogy ez a beteg még indukció alatt is rezisztens a bortezomibdal és a lenalidomiddal szemben. Annak ellenére, hogy az auto-SCT után nagyon jó PR-t ért el, betegsége az auto-SCT után 9 hónappal előrehaladt, ami erősen refrakter myelomára utal, amit az agresszív betegség progressziója bizonyít, gyorsan növekvő IgG-szint mellett. Ezenkívül, mivel betegsége az auto-SCT után 9 hónapon belül előrehaladt, a myeloma sejtek valószínűleg kemorefraktívak voltak a bortezomib, a talidomid és a lenalidomid mellett nagy dózisú melfalán mellett. Sajnos a karfilzomib és a pomalidomid nem állt rendelkezésre. Ezért a hagyományos kemoterápia helyett új terápiákat fontolgattak a relapszusért.
A bendamustin a nitrogén mustár és a benzimidazol kémiai hibridje, ezért mind alkilező, mind purin analóg tulajdonságokkal rendelkezik. A bendamustin nem keresztrezisztens más kemoterápiákkal szemben, és hatásos indolens non-Hodgkin-limfóma, CLL és mielóma esetén. Korábban kimutattuk, hogy a bortezomib helyreállíthatja a kemoszenzitivitást a myelomában szenvedő betegeknél, akik több kemoterápiával szemben refrakterek, 4 ezért a Bortezomib-alapú terápiában gyors progresszív relapszusú VBD-t alkalmaztak ebben a betegben. Ez a PR kombináció más alkilezőszerekkel szembeni keresztrezisztenciájával összhangban bendamustint eredményezett. A bendamustin/prednizolon relapszusban/refrakter myelomában végzett legújabb vizsgálata valóban szerény válaszarányt mutatott, 13 de a bortezomib bendamustinnal és dexametazonnal történő kombinációjával sokkal magasabb válaszarányt (60%) érnek el. 14 Végül a bortezomib bortezomib-refrakter betegeknél történő alkalmazásának indoklása in vitro és in vivo adatokon alapul, amelyek bemutatják az alkilező szerek kemoszenzitivitásának helyreállítását kemorezisztens myeloma sejtekben. 4
A RAS-RAF-MEK-ERK jelzés funkcionálisan igazolt aktiválása a KRAS/NRAS mutáció vagy a RASSF1A hipermetiláció helyett a BRAF V600E mutációval társulhat. A szorafenib nem elég erős ahhoz, hogy a BRAF-mutáció miatti RAS-aktiváció esetén jelentős választ váltson ki, ezért vemurafenib-kísérletre van szükség. A VBD aktív kezelés még mielómás betegeknél is, akik rezisztensek a bortezomib vagy lenalidomid alapú kezelési módokra, kivéve a nagy dózisú melfalánt.
beleegyezés
A jelentés közzétételéhez írásos tájékoztatáson alapuló beleegyezést kapott a beteg. Az írásbeli hozzájárulás egy példányát megtekintheti a folyóirat főszerkesztője.
- Gyermekgyümölcs tea mézzel a jó alváshoz, 20x2 g Gyógyteák
- Dexametazon és a mellékvese szuppressziójának kockázata myeloma multiplex leukémia esetén
- Bortezomib STADA 2,5 mg ml
- Szeretne egy jó általános áttekintést Próbálja ki ezt a 7 lehetőséget
- Szeretnék havonta 50 vagy 100 eurót megtakarítani, ajánlatot kell vennem a banktól, különben nem jó ötlet;